بیماریهای انگلی
تازه های انگل شناسیبیماریهای انگلی
تازه های انگل شناسیبیوتکنولوژی و واکسنهای نسل دوم ضد انگلهای لیشمانیا
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
درگذشت استاد فرزانه آقای دکتر ناصرملک نیا
الی الله المصیر
درگذشت استاد فرزانه آقای دکتر ناصرملک نیا را به جامعه علمی ایران تسلیت می گوئیم.
کرم اسکاریس
|
دیدکلی
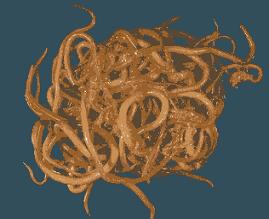 |
ساختمان کرم روده
مخرج عبارت از یک شکاف عرضی است که نزدیک انتهای خلفی در سطح شکمی قرار دارد. انتهای خلفی کرم نر کاملا خمیده بوده و دارای دو سیخک تناسلی میباشد که از سوراخ تناسلی نر واقع در داخل مخرج بیرون میآید. کرم ماده راست تر بوده و منفذ تناسلی آن در وسط سطح شکمی و در فاصله 1.3 از انتهای قدامی بدنش واقع است.
لوله گوارش
- دهان
- یک حفره دهانی
- حلق عضلانی یا مری به درازای تقریبا 13 میلیمتر که عمل آن مکیدن و کشیدن غذا است.
- یک روده باریک و دراز که غیر عضلانی است و از لایهای مرکب از سلولهای آندودرمی بلند که غذای گوارش یافته را جذب میکند، تشکیل و از خارج بوسیله کوتیکولی پوشیده شده است.
- یک روده راست کوتاه که مواد زاید را از مخرج تخلیه میکند.
 |
سایر دستگاهها
اندامهای گردش خون و دمزدن در حیوان وجود ندارد. قسمت داخلی هر خط جانبی دارای یک مجرای وازنشی (دفعی) است. هر دو مجرای وازنشی از سوراخ کوچکی واقع در پشت دهان و در وسط سطح شکمی به خارج تخلیه میشود. یک حلقه عصبی اطراف مری را احاطه میکند. این حلقه عصبی به 6 عصب قدامی کوتاه و 6 طناب عصبی خافی متصل میگردد. یک طناب عصبی بزرگتر پشتی و یکی هم شکمی در امتداد خط طولی بدن قرار دارد. برآمدگیهای مختلف که در سطح بدن وجود دارد، احتمالا عمل حسی را انجام میدهد.دستگاه تولید مثل
هر اندام تولید مثل عبارت از لوله باریکی است که انتهای داخلی آن مسدود بوده و قطر آن تدریجا زیاد میشود. غدد تناسلی و مجرای تولید مثل به هم متصل و ممتد میباشد. دستگاه تولید مثل نر شامل بیضه ، مجرای ناقل اسپرمی ، کیسه اسپرمی ، مجرای انزالی و کیسه محتوی دو سیخک تناسلی است. دستگاه تولید مثل ماده شامل 2 تخمدان ، یک اویدکت یا لوله تخمی و یک رحم است.دو شاخه رحم هم در یک مهبل کوتاه به هم متصل میشود. مهبل به منفذ تناسلی ماده باز میگردد. کرمهای نر و ماده در داخل روده میزبان جفت گیری میکنند. یک ماده بزرگ میتواند یکباره حاوی 27000000 (بیست و هفت میلیون) تخم باشد و روزانه دویست هزار یا بیشتر تخم بگذارد. تخمها از حیوان ماده خارج شده و به داخل روده میزبان میریزد و همراه با مدفوع بیرون میریزد.
وضع طبیعی
کرم روده یا آسکاریس انگلی است که در روده میزبانش زندگی میکند و به همین جهت تعیین اعمال مختلف زیستی یک انگل داخلی هنگامی که در مسکن طبیعی خود به سر میبرد، کار مشکلی است. لذا احتمال دارد که استنباطات زیر درست باشد.- کوتیکول کرم زنده را در برابر شیرههای گوارشی میزبان حفظ میکند.
- غذا از مواد نیمه مایع روده میزبان بدست میآید و بوسیله مری عضلانی کرم به داخل کشیده میشود. پس از گوارش از دیواره روده عبور کرده به توسط مایع موجود در فضای بدنی در بافتهای دیگر توزیع و تقسیم میگردد.
- تنفس به شکستن یا تجزیه شدن گلیکوژن در داخل بدن کرم بستگی دارد. زیرا اکسیژن آزاد محتویات روده میزبان بسیار کم است.
 |
سیر تکاملی
قبل از آن که تخمها بتوانند میزبان دیگری را آلوده کنند، لازم است از نظر سیر تکاملی مرحلهای را بگذراند. همچنین تخمهای مزبور در شرایط نامساعد مثلا سرما میتوانند ماههای بسیاری در حال بی حرکتی و خواب باقی ماند. سیر تکاملی در جای گرم ، مرطوب و سایه دار به 2 یا 3 هفته وقت احتیاج دارد. اگر این تخمهای جنین دار (حاوی کرمهای جنینی) بوسیله میزبان مناسبی ، ضمن غذا یا آب خورده شود، به طرف معده حرکت میکند و در آنجا لاروها از تخم بیرون میآیند و به داخل سیاهرگها یا عروق لنفی دیواره روده نفوذ مینمایند.سپس به طرف کبد و قلب و مویرگهای ریوی به گردش در میآیند و ضمنا از لحاظ اندازه نیز بزرگ میشوند. ظرف چند روز لاروها به داخل راهها یا گذرگاههای هوایی آمده از نای ، مری و معده مجددا به طرف روده حرکت میکنند. در روده به صورت کرم رسیده و بالغ در میآیند. برای تکمیل و اتمام دوره زندگی کرم روده میزبان واسطه لازم نیست.
میزبان کرم آسکاریس
میزبان این کرم انسان و خوک میباشد. کرمهایی که در انسان و خوک وجود دارند، از نظر ساختمانی به هم شبیهاند، ولی از نظر فیزیولوژیکی اختلاف دارند. بدین ترتیب که تخمهای آلوده کننده کرم روده انسانی (کرم روده اطفال) معمولا در خوکها تولید کرم نمیکنند و بر عکس خوکهای جوان (بچه خوک ) معمولا لاروها را از خاکهای آلوده در طویله یا از پستان کثیف ماده خوک در موقع شیر خوردن میگیرند. خوکهای بالغ در برابر آلودگی نسبتا مصون هستند.آلودگی انسان به کرم روده امر شایع و رایج است و اکثر مردم نواحی روستایی مبتلا هستند. کرمها ممکن است ترشحات سمی در روده تولید کنند یا به علت کثرت تعداد کرمها در روده ، مانع و انسداد بوجود آید. گاهی اوقات کرمها به طرف دهان یا بینی مهاجرت میکنند و حتی دیواره روده را به منظور رسیدن به سایر اندامها سوراخ میکنند. از این رو کسالت وخیم و یا مرگ را برای میزبان به بار میآورند.
 |
عوارض آسکاریدوز
وجود تعداد زیاد کرم آسکاریس ، مهاجرت و یا تجمع آنها در رودهها گاهی سبب ایجاد عوارض شدید میشود. این عوارض عبارتند از انسداد رودهها ، ابتلای کیسه صفرا ، پانکراتیت و آپاندیست حاد و سوراخ شدن رودهها. علایم انسداد روده ها شامل درد ناگهانی و پیچش شکم همراه با استفراغ ، اتساع شکم و مشاهده انسداد در عکسبرداری با اشعه ایکس است.تشخیص
تشخیص آلودگی به کرم بالغ با آزمایش مدفوع و مشاهده تخم به آسانی صورت میگیرد . در این مرحله تشخیص انسداد روده به علت آسکاریس با لمس شکم و تودههای نرم و متحرک در زیر انگشتان ممکن است. تشخیص استقرار کرم آسکاریس در محلهای دیگر بدن فقط در هنگام عمل جراحی امکان دارد. بهترین روش آزمایش مدفوع برای تشخیص آسکاریس استفاده از روش کاتوکاتز است.درمان
چند داروی موثر بر آسکاریس عبارتند از: ترکیب مبندازول ، ترکیب لوامیزول و ترکیبات پیرانتل پاموت
گرفته شده از: شبکه رشد
شناسایی نخستین مورد ابتلا به انگل گانگیلونما در ایران
برای اولین بار در ایران گزارشی مبنی بر مشاهده یک مورد بیماری انگلی خاص منتشر شده است که میتواند هشداری جدی برای شیوع بیماریهای کمتر شناخته شده مشترک میان انسان و دام در ایران به شمار رود.نشریه علمی "کرم شناسی" در شماره جدید خود در ماه ژانویه ۲۰۰۷ گزارش مشترکی از دو پژوهشگر ایرانی و یک محقق آمریکایی منتشر کرده که برای اولین بار مراجعه یک بیمار زن ایرانی با نشانههای آلودگی به انگل "گانگیلونما" را اعلام کردهاند.
انگل گانگیلونما که در حقیقت یک کرم حلقوی به شمار میرود به صورت نادر به انسان سرایت میکند و بیشترین موارد وقوع آن تاکنون در شوروی سابق، اروپا و بخشهایی از خاورمیانه گزارش شده است.
بیمار زن ایرانی که اکنون معالجه شده پیش از آن بارها با احساس خزیدگی در زیر پوست به پزشک عمومی مراجعه کرده بوده اما پزشکان به وی می گفتند که او دچار "توهم" است و در نتیجه این تشخیص نادرست، برای او داروهای روانی تجویز می کرده اند.
اما مراجعه بیمار به مرکز تحقیقات بهداشت عمومی دانشگاه علوم پزشکی تهران منجر به شناسایی انگل در ناحیه گردن بیمار و در نتیجه گزارش یک بیماری انگلی نادر در ایران شده است.
آقایان مولوی و مسعود از دانشگاه علوم پزشکی تهران و آقای گوتیهرز از دانشگاه اوهایو در گزارشی که منتشر کردهاند از وجود میزبانان ناقل نظیر حشرات و سپس پرندگان برای انگل گانگیلونما نام بردهاند. با این حال امکان انتقال مستقیم انگل با خوردن سبزیجات آلوده نیز وجود دارد.
به عقیده پژوهشگران آلودگی در ایران به احتمال زیاد ناشی از آلودگی دامها و استفاده از گوشت دامهای آلوده توسط مردم است. بر اساس همین گزارش ۴۵ درصد از گاوها و ۲۱ درصد از گوسفندان در ایران آلوده به انگل گانگیلونما هستند.
عمده گزارشهای پزشکی موجود نشان دهنده وجود تنها یک انگل ماده در بدن بیمار بوده است اما بنا به گزارش جدید وجود دو انگل نر و ماده در بدن بیمار ایرانی اثبات شده است که نشان دهنده احتمال شیوع بیشتر آلودگی و در نتیجه تماس بیشتر افراد با منابع آلودگی است.
آنچه تاکنون در منابع پزشکی از آن به عنوان علائم آلودگی با گانگیلونما نام برده شده احساس وجود جسمی خزنده در زیر پوست گردن، حلق و حتی زبان است.
حذف امتحان جامع مقطع دکترا
سلام امروز روزنامه همشهری خبر جالبی نوشته بود .حذف امتحان جامع مقطع دکترا به نظر قراره در کمسیون آموزش مجلس مطرح شود . به نظر بمده هم این امتحان زیاد هم لازم به نظر نه میرسه حالا چرا؟؟؟؟؟؟؟؟
شرط قبولی در یک درس رو ۱۴ است.و وعدل زیر ۱۵ هم مشروط است پس یه دانشجوی دکترا باید سواد داشته باشد تا بتونه اینا رو کسب کنه؟منتظر نظراتتون هستم.
Leishmania infantum
ELISA kit for the diagnosis of visceral leishmaniosis in humans and dogsParasitology and clinical relevance
The parasites of the genus Leishmania are intracellular protists transmitted by an insect vector. Traditionally three forms of leishmanioses are clinically distinguished : One of these, visceral leishmaniosis, is caused by Leishmania infantum in the Mediterranean area and in South America and by L. donovani in Eastern Africa and in Southern Asia. This infection affects millions of individuals and is frequently lethal if left untreated. Recently a growing number of patients developed visceral leishmaniosis during a co-infection with HIV. Epidemiologically, the domestic dog is very sensitive to infection by L. infantum and is an important reservoir host for the transmission of the human disease. The culture of the parasite from biopsies or a direct detection of amastigotes in tissue smears are definitve proof for the presence of the parasite. However, as the antibody titers are usually elevated in the absence of HIV co-infection, serology is conveniently used as a less invasive procedure for the diagnosis and the follow-up during treatment of visceral leishmaniosis
سالم سازی سبزیجات

● اهمیت مصرف سبزیجات
سبزیجات و میوهها سرشار از ویتامینهای گروه A و گروه C بوده و همچنین حاوی مقداری ویتامین B ، آهن و مقدار قابل توجهی فیبر هستند. سبزیجات بخاطر نقش مؤثرشان در تامین سلامت انسان یکی از گروههای مهم مواد غذایی محسوب میشوند و برای حفظ مقاومت بدن در برابر عفونتها یا ترمیم زخمها، دید در تاریکی و سلامت پوست ضروری هستند. به همین علت توصیه شده است همیشه همراه غذا از سبزیجات تازه نیز استفاده شود.
● آلودگی سبزیجات
سبزیجات اغلب به دلیل استفاده از کودهای انسانی و حیوانی، آب آلوده و تماس حیوانات به عوامل بیماریزا آلوده میشوند. در صورت مصرف چنین سبزیجاتی خطر ابتلا به بیماریهایی نظیر وبا، حصبه، هپاتیت، اسهال خونی و بیماریهای انگلی نظیر کیست هیداتیک و آسکاریس وجود دارد. لذا لازم است به خاطر بر طرف نمودن آلودگیهای فوق سبزیجات قبل از مصرف سالمسازی شوند. سبزیجاتی که به صورت خام در تزیین غذا و یا همراه ساندویچ و سالاد استفاده میشوند نیز بایستی سالم سازی و سپس مصرف شوند.
● مراحل تمیز کردن و سالمسازی سبزیجات
سالم سازی سبزیجات شامل چهار مرحله اساسی است: پاکسازی، انگلزدایی، گندزدایی، شستشو
▪ مرحله اول _ پاکسازی
ابتدا سبزیجات را بخوبی پاک نموده و مواد زاید و غیر قابل مصرف آنرا جدا و سپس خوب شستشو دهید تا گل و لای و مواد زاید از سبزیجات پاک گردد.
▪ مرحله دوم _ انگلزدایی
پس از خاتمه مرحله پاکسازی، سبزی پاک شده را در یک ظرف ۵ لیتری آب ریخته و بازاء هر لیتر آب سه تا پنج قطره مایع ظرفشویی به آن اضافه کنید. قدری بهم زده تا تمام سبزیجات در کفاب غوطهور شود و پس از چند دقیقه، آنها را به آرامی از روی کفاب جمعآوری کنید. ظرف و سبزی را مجددا با آب سالم خوب شستشو دهید تا تخم انگلها و باقیمانده مایع ظرفشویی از آنها جدا شود.
▪ مرحله سوم _ گندزدایی
برای گندزدایی و از بین بردن میکروبهای بیماریزا بهتر آنست که از مواد گندزدایی مجاز موجود در داروخانهها یا فروشگاههای مواد غذایی و طبق برچسب موجود بر روی آن استفاده شود اما چنانچه در دسترس نبود، یک گرم (نصف قاشق چایخوری) پودر پرکلرین را در ظرفی محتوی ۵ لیتر آب بریزید تا کاملا در آب حل گردد. محلول مذبور ضدعفونی کننده میباشد. سبزیجات انگلزدایی شده مرحله قبلی را به مدت ۵ دقیقه در این محلول قرار دهید.
▪ مرحله چهارم _ شستشوی نهایی
پس از اجرای گندزدایی سبزیجات آنها را مجددا با آب سالم و فراوان بشویید تا باقیمانده کلر یا مواد گندزدای بکار رفته کاملا از سبزیجات جدا شوند. پس از شستشوی نهایی سبزیجات را میتوان مصرف نمود.
شبکه رشد
پژوهشگران ایرانی موفق به ساخت واکسن سالک شدند
|
رئیس آزمایشگاه انگلشناسی مولکولی انستیتو پاستور ایران از موفقیت پژوهشگران کشورمان در ساخت نخستین واکسن لیشمانیوز پوستی و احشایی با استفاده از ژن A2rel خبر داد. | ||
انجمن انگل شناسی ترکیه

Tıbbi ve Veteriner Parazitoloji alanlarında yayımlanan makalelerin (deneysel, gözlemsel araştırma, klinik denemeler, olgu sunumu ve derleme niteliğinde) yanısıra, Biyoloji bilim alanında çalışan bilim insanlarının ürettiği Parazitoloji konularını kapsayan makaleler de kabul edilmektedir
Türkçe ve İngilizcedir. Türkçe makaleler ingilizce başlık, özet ve anahtar kelimeler; ingilizce makaleler ise türkçe başlık, özet ve anahtar kelimeler içermektedir.
کشف مکانیسم مقاومت دارویی در لیشمانیا
محققان هندی مکانیسم مقاومت دارویی انگل لیشمانیا، عامل بیماری لیشمانیازیس احشایی یا کالاآزار، را شناسایی کردهاند. مقاومت لیشمانیا دنوانی به داروی سدیم اسیبوگلوکونات ( با نام تجاری پنتوستام)، داروی معمول برای درمان بیماری، در هند بسیار گسترده است. محققان دریافتند که در سلولِ انگلهای مقاوم، غلظت تیولها- ترکیبات حاوی گوگردـ افزایش مییابد. آنها همچنین آنزیم تریپانوتیون ردوکتاز و نیز ژن MRPA را در انگلهای مقاوم شناسایی کردند. این سه فاکتور موجب افزایش برداشت و حذف دارو از داخل سلول انگل و در نتیجه، مقاومت دارویی میگردد. بر اساس آمار سازمان جهانی بهداشت، حدود ۵۰ درصد موارد بیماری لیشمانیازیس احشایی فقط در هند رخ میهد. بنگلادش، نپال و سودان از دیگر مناطق عمده این بیماری در جهان هستند. در بیشتر مناطق روستایی بیهار، مقاومت دارویی آنقدر بالاست که این دارو، حتی با دوزی ۶-۸ برابر دوز معمول، تنها میتواند یک سوم از بیماران را بطور موثر درمان کند. با توجه به اینکه لیشمانیازیس احشایی عمدتاً افراد فقیر را مبتلا میکند، از این رو علیرغم ظهور چندین داروی جدید، پنتوستام به خاطر قیمت پایین در درمان بیماری اهمیت زیادی دارد. این محققان به مهار مقاومت دارویی امیدوارند. آنزیم گلوتاتیون ردوکتاز در افزایش غلظت تیولها در سلولها نقش اساسی دارد و لذا میتوان از یک مهارکننده این آنزیم برای کاهش سطح تیول و در نتیجه مهار مقاومت دارویی استفاده کرد. آزمایش این مهارکنندهها روی انگل لیشمانیا قدم بعدی در این زمینه است. این مطالعه در شماره آوریل مجله پزشکی گرمسیری و بهداشت آمریکا منتشر شده است
Reference: American Journal Of Tropical Medicine 76, 681 2007

